עמוד 17 בספר:
בהתייחס לגרף האנרגיה, חשוב להדגיש לתלמידים שהמגמה הכללית של גרף זה זהה לכל זוג אטומים שמתקרבים זה לזה. כאשר האינטראקציה היא בין אטום כלור לאטום נתרן, הקשר שיווצר יהיה קשר יוני, קשר חזק יחסית לקשר בין שני אטומי כלור למשל, פליטת האנרגיה תהיה רבה יותר, ולפיכך, נקודת המינימום של הגרף תהיה נמוכה יותר מהמקרה של שני אטומי כלור. אם נתייחס לקשר יחיד, כפול ומשולש בין שני אטומי פחמן, על התלמידים להבין שהקשר הכפול חזק יותר מהיחיד והמשולש חזק מהכפול, וזאת על פי חוק קולון. לפיכך, גרף האנרגיה יהיה "עמוק" יותר ככל שהקשר חזק יותר כיוון שאנרגיית הקשר גדולה יותר. כמו כן, אורך הקשר קצר יותר במקרה של הקשר המשולש בהשוואה לכפול וליחיד ודבר זה מתבטא ב"תזוזה" על ציר ה- X.
בדוגמא שמובאת להלן, מתאר הגרף את שינויי האנרגיה כפונקציה של המרחק בין שני אטומי ארגון.
נדון כעת באינטראקציות שבין שני אטומי ארגון.
בתרשים שלפניכם ניתן להבחין בשתי עקומות: העקומה התחתונה- המתארת את אנרגיית המערכת (שני אטומי מימן) כתלות במרחק בין אטומי המימן בתהליך היווצרותה של מולקולת מימן ולעומתה, העקומה העליונה, המתארת את השתנות אנרגיית המערכת (שני אטומי ארגון) כתלות במרחק בין שני אטומי ארגון. גם במקרה של שני אטומי הארגון, נקודת המינימום מתארת מצב בו קיים איזון בין כוחות הדחייה לבין כוחות המשיכה. ניתן לראות על פי נקודות המינימום בשתי העקומות, כי מחד, בין אטומי הארגון קיימת אינטראקציה חלשה יחסית לזו שבין שני אטומי מימן בנקודת האיזון – האטומים קרובים, אבל לא יוצרים מולקולה. אולם מאידך, אלו הם הכוחות האחראיים על כך שאטומי ארגון מוחזקים יחד בנוזל ובמוצק.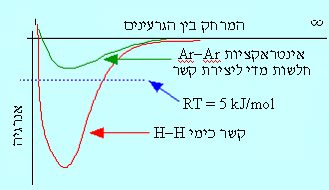
עמוד 29 בספר:
כאשר דנים בהשוואה בין חוזקי קשרים, בין אטומים שונים, צריך לקחת בחשבון ששינוי זהות האטום הקשור לא משנה רק את האלקטרושליליות אלא תכונות נוספות של אותו אטום כמו למשל גודלו, המבנה האלקטרוני שלו ועוד.
הסקלה שמסכמת את הפריסה של סוגי הקישור השונים בהתייחס לחוזק הקשר בין שני אטומים, היא סקלה שמצד אחד מספקת לתלמיד נקודת אחיזה וראייה כללית של "מיקום" סוגי הקישור השונים מבחינת חוזקם, אך מצד שני אינה קובעת באופן נחרץ שקשר קוטבי תמיד חזק יותר מקשר קוולנטי טהור.
דוגמאות לכך הן למשל:
א. השוואת חוזקי הקשר מימן-מימן במולקולת מימן (436 קילוג'ול למול) לקשר מימן כלור במולקולת מימן כלורי (431 קילוג'ול למול).
ב. פחמן פחמן (346 קילוג'ול למול) לעומת פחמן-כלור (327 קילוג'ול למול).
על מתכות – מתכת כתכונה
פיזיקאים נוהגים להגדיר את המושג "מתכת" כתכונה. על פי תפיסתם, חומר שמוליך חשמל במצב המוצק עקב קיומם של אלקטרונים חופשיים, הוא מתכת. החומר לא חייב להיות יסוד, הוא לא חייב להיות ניתן לריקוע ולכן, על פי תפיסתם, לא ניתן לתאר את כל המתכות על פי מודל אחיד ברמה הננומטרית. התכונה היחידה שחייבת להתקיים בחומר היא הולכה חשמלית במצב מוצק על ידי אלקטרונים חופשיים. נביא דוגמאות לכך במדריך למורה.
ייצור זכוכית:
חומרי הגלם לייצור זכוכית הם, בדרך כלל, חול של קוורץ נקי, סודה ואבן גיר. מערבבים חומרים אלה היטב ומחממים עד לכ- 1600oC :
-
Na2CO3(s) + SiO2(s) → Na2SiO3(s) + CO2(g)
(CaCO3(s) + SiO2(s) → CaSiO3(s) + CO2(g
את הסיליקטים של נתרן וסידן מתיכים עם חול שנלקח בעודף. זכוכית היא לא חומר אחד אלא סגסוגת של מספר חומרים. הרכב מקורב של זכוכית חלונות רגילה (זכוכית נתרן) אפשר לבטא כך: Na2O•CaO•6SiO2 .
אם מחליפים סודה ב- K2CO3(s) , מקבלים זכוכית עמידה יותר לחום (זכוכית כימית, זכוכית אשלגן). הרכב מקורב של זכוכית חלונות רגילה (זכוכית נתרן) אפשר לבטא כך: K2O•CaO•6SiO2.
אם בתור חומרי גלם לוקחים K2CO3(s), PbO(s) וחול, מקבלים זכוכית קריסטל. זכוכית זו שוברת חזק את האור ולכן משמשת לייצור עדשות ומנסרות, וגם כלי קריסטל.
מחול נקי מקבלים זכוכית קוורץ. כשחול מותך מתקרר נוצר חומר דמוי זכוכית. שלא כזכוכית רגילה, הנפח של זכוכית קוורץ משתנה מעט מאוד עם שינוי טמפרטורה. כלי זכוכית כאלה אפשר לחמם עד טמפרטורה גבוהה ולזרוק למים קרים, בלי שהזכוכית תיסדק. מזכוכית קוורץ מייצרים כלי מעבדה. תכונה אופיינית נוספת של זכוכית זו היא יכולת להעביר קרניים אולטרה-סגולות, לכן מזכוכית זו מייצרים נורות קוורץ שיש להן שימוש ברפואה.
לקבלת זכוכיות צבעוניות מוסיפים לחומרי הגלם תחמוצות של מתכות מתאימות. כך למשל, אם מוסיפים תחמוצת קובלט (II) מקבלים זכוכית כחולה. תחמוצת כרום (III) מקנה לזכוכית צבע ירוק. תחמוצת נחושת מקנה לזכוכית צבע כחול-ירוק. אם מוסיפים מעט אבקת זהב מקבלים זכוכית בצבע רובין.
כשמקררים זכוכית מותכת היא לא הופכת מייד למוצק אלא באיטיות נעשית יותר ויותר צמיגה. הודות לתכונה זו אפשר לקבל צורות שונות של מוצרי זכוכית. עיבוד הזכוכית נעשה בדרכים שונות: ניפוח (נורות, בקבוקים), עיבוד בעזרת מכבש (כפתורים), ערגול (זכוכית מראות), מתיחה (עלי זכוכית, צינורות זכוכית מקלות זכוכית).
מזכוכית מייצרים גם חוטי זכוכית דקים. השימוש בהם נעשה בייצור סיבי זכוכית ובדים. בדי זכוכית משמשים מבודדים של חום וחשמל. משלבים סיבי זכוכית ופולימרים בייצור פולימרי-זכוכית שהחוזק שלהם דומה לזה של פלדה.


