חיסונים מונעים
תפנית חדה בחקר תורת החיסון, ובכלל זה בתחום הפיתוח של תרכיבי חיסון, חלה בעקבות זיהוי המיקרואורגניזמים הפתוגניים (גורמי המחלות) כמו חיידקים, נגיפים וטפילים ופיתוח תהליכים להחלשתם בתנאי מעבדה.
חיסון פעיל בגורם מחלה מוחלש או מומת:
היה זה לואי פסטר*[1] שהציע גישה יעילה לחיסון באמצעות גורמי מחלה מוחלשים. פסטר, שייעד לעצמו עתיד כמורה, למד כימיה באוניברסיטה והיה לפרופסור לכימיה. הוא גילה עניין רב גם בנושאים ביולוגיים. לזכותו נזקפות תגליות רבות וחשובות. ביניהן נזכיר את המחקר שהוכיח בהצלחה, כי יצור חי איננו יכול להתפתח באופן ספונטני, אלא כל יצור חי מוצאו מיצור חי אחר שקדם לו; וכן את המחקר שבו פיתח תהליך להחלשה מכוונת של מיקרואורגניזמים גורמי מחלה על ידי גידולם במעבדה בתנאים בלתי אופטימליים*[2]. מסקנותיו מתצפיות בדרכים לגונן על אנשים מפני מחלות מידבקות ותוצאות פיתוח התהליך להחלשת חיידקים או נגיפים הובילו אותו להשערה הזאת: ניתן ליצור במעבדה גורם מחלה מוחלש, שאיבד את אלימותו, ועם זאת הוא יפעיל את מערכת החיסון נגדו כך שזו תתגבר גם על הגורם האלים אם זה יחדור לגוף.
בשנת 1880 דיווח פסטר לקהילה המדעית על הצלחתו להקנות לעופות חיסון מפני מחלת הכולרה (chicken cholera) על ידי הזרקה של גורמי מחלה מוחלשים. כעבור שנה הוא הצליח לפתח תרכיב חיסון נגד מחלה אחרת, מחלת הגחלת (anthrax), שהשמידה עדרי בקר רבים בצרפת ואיימה על החקלאות*[3]. בניסוי מבוקר שנמשך מספר שבועות הוא הוכיח, שבין חיות הכפר שנחשפו לגורם המחלה האלים מתו אלה שהוא לא חיסן, ואילו המחוסנות לא חלו בגחלת*[4]. מכאן שהשערתו של פסטר אומתה. הכנתו של תרכיב חיסון נוסף וחשוב, שזיכה את פסטר בפרסום רב, מתוארת בקטע ההרחבה.
ממצאיו של פסטר הדגימו את השימושיות הרבה שיש לגורמי מחלה מוחלשים במניעת מחלות. ממצאים שהתקבלו זמן קצר אחר כך הוכיחו, שגם גורמי מחלות מומתים יכולים לשמש למטרה זאת. ממצאים אלה קידמו את התקווה,
שכל מחלה זיהומית אשר הצליחו לבודד את הגורמים לה ניתנת לריסון בעזרת תרכיב חיסון. חיסון הנרכש כתוצאה מפלישה של גורם מחלה אלים או ממתן תרכיב (מוחלש או מומת) לגופו של אדם או בעל חיים נקרא חיסון פעיל. חיסון פעיל מפעיל את מערכת החיסון, מותיר אחריו זיכרון חיסוני ספציפי, ומונע את הופעת המחלה.
באיור שלפניך מוצג באופן סכמטי העיקרון שעליו מבוסס חיסון פעיל:
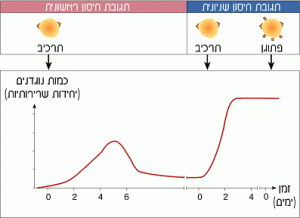
בסוף המאה ה- 19 נעשו ניסויים ליישם את גישתו הטיפולית של פסטר בכל המחלות. רבים מהם נכשלו. במקרים רבים התקשו החוקרים לזהות ולבודד את גורמי המחלה. מאוחר יותר התברר, כי בחלק מאותם מקרים הגורמים הם נגיפים (או טפילים). במקרים אחרים, כמו במקרה של ה- Treponema pallidum – החיידק הגורם למחלת העגבת – אף שזוהה גורם המחלה לא הצליחו לגדלו בתרבית במעבדה לצורך הכנת תרכיב. כמו כן היו מקרים, כמו במחלת השחפת, שהצליחו לגדל את החיידק במעבדה ולהחלישו, אולם הזרקת גורם המחלה המוחלש לא הקנתה הגנה מפני הגורם האלים.
תחלופה נגישה לשאלות
חיסון סביל:
במסגרת החיפושים אחר דרכים לריפוי אנשים ממחלת הדיפתריה (הקרמת) הקטלנית נערכו ניסויים רבים. א' רו (E. Roux), תלמידו של פסטר, וא' ירסן ׁׁׁׁׂ(A .Yersin) הוכיחו לראשונה, כי הרעלן המופרש מחיידק הדיפתריה
(diphteriae Corynebacterium) – ולא המיקרואורגניזם עצמו – גורם למחלת הדיפתריה.
תחלופה נגישה לשאלות
א' פון ברינג (E. Von Behring), שהיה רופא צבאי ועוזרו של קוך, וש' קיטזטו (S. Kitasato) הניחו שתי הנחות יסוד:
א. חייבת להימצא תרופה שהזרקתה תנטרל את הגורם לדיפתריה. כדי לבדוק זאת הם ניסו לרפא חיות בעזרת למעלה מ- 30 חומרים שונים. בכל המקרים החיות מתו.
באחד הימים, במקרה, הוזרקה לחלק מהחיות החולות תרופה בשם -tri iodine. חלק מהחיות המוזרקות בתרופה זאת החלימו. זאת ועוד, החיות המחלימות היו מחוסנות מפני דיפתריה גם כשהוזרקה לגופן מנה קטלנית של הרעלן!
האם נמצאה תרופה אשר תציל את האנושות מדיפתריה? לא! מקבלי התרופה סבלו מתופעות-לוואי שליליות שסיכנו את חייהם.
ב. הגורם המחסן מפני דיפתריה נמצא בדם. כדי לבדוק זאת הם ערבבו את רעלן הדיפתריה עם סרום*[5] שהופרד מדמן של חיות מחוסנות כנגד דיפתריה.
התערובת הוזרקה לחיות ניסוי נורמליות. הניסוי ותוצאותיו מסוכמים בטבלה שלפניך:
| קבוצה | הזרקה ראשונה | הזרקה שנייה (כעבור מספר שבועות) | תוצאות |
|---|---|---|---|
| 1 | מנה קטלנית של רעלן הדיפתריה | החיות חלו בדיפתריה ומתו | |
| 2 | מנה קטלנית של רעלן הדיפתריה ותרופה נגד דיפתריה | מנה קטלנית של רעלן הדיפתריה | החיות לא חלו |
| 3 | סרום של חיות מקבוצה 2 (לאחר 2 הזרקת) ומנה קטלנית של רעלן הדיפתריה | החיות לא חלו | |
| 4 | סרום של חיות נורמליות (לא מחוסנות) ומנה קטלנית של רעלן הדיפתריה | החיות חלו בדיפתריה ומתו |
חיסון המקנה הגנה מפני מחלה והמתקבל על ידי הזרקה של סרום מפרט מחוסן לפרט לא מחוסן נקרא חיסון סביל. חיסון זה מקנה הגנה מיידית מפני הגורם הפתוגני; אבל השפעתו חולפת, והוא איננו מותיר זיכרון חיסוני.
פון ברינג וקיטזטו כינו את החומר אשר מצוי בסרום של החיות המחוסנות ומגן עליהן מפני דיפתריה בשם -anti , שפירושו גוף נגדי. בעברית הוא נקרא נוגדן. בדצמבר 1891 הגיעה למרפאתו של פון ברינג ילדה חולת דיפתריה שמצבה הלך והדרדר מרגע לרגע. פון ברינג החליט לנסות ליישם את עקרון החיסון הסביל, שגילה שנה קודם לכן במחקרו על חיות ניסוי במעבדה. הוא הזריק לילדה סרום שנלקח מכבשה מחוסנת נגד רעלן הדיפתריה. כעבור מספר שעות ניכרו בילדה סימני התאוששות; היא ניצלה והחלימה. בעקבות זאת ניצלו חייהם של ילדים רבים אחרים שזכו לטיפול רפואי דומה. היה זה הגילוי הראשון של נוגדנים, שהם תוצר מרכזי של מערכת החיסון. גילוי זה מהווה אבן דרך במחקר האימונולוגי.

פון ברינג ( -1917), וארליך (-1915). שני החוקרים קיבלו פרס נובל לרפואה ופיזיולוגיה (ברינג ב- 1901 וארליך ב- 1908) על תרומתם לחקר החיסון.
ממצאיו של פון ברינג (בטיפול בסרום ספציפי נגד רעלן) עוררו עניין רב בקרב הרופאים. נעשה ניסיון ליישם את שיטת החיסון הסביל בטיפול במחלות רבות. אולם נמצא, כי טיפול מסוג זה מתאים בעיקר לריפוי חולי דיפתריה וחולי טטנוס; וזאת בתנאי שהטיפול ניתן בשלבים הראשוניים של המחלה.
גם כיום במצבים מסוימים מטפלים בחולה בחיסון סביל. להלן שתי דוגמאות לכך:
- מצב שבו נדרשת הגנה מיידית: לדוגמה, קיים חשש שאנשים נחשפו לחומר רעיל במיוחד, כמו רעלן הטטנוס או ארס נחשים. במצב כזה אין זמן לחכות עד שיווצר חיסון פעיל.
- מצב שבו הזרקה של גורם מחלה (מוחלש או מומת) לא תעורר תגובה חיסונית יעילה נגדו. לדוגמה, חולים המטופלים בתרופות המדכאות את הפעילות של מערכת החיסון.
חיסון סביל מופיע גם בטבע; נוגדנים של האם מועברים לעוברה, ומגנים על הרך הנולד בחודשים הראשונים לחייו מפני אותם גורמי מחלה שהאם הייתה מחוסנת נגדם. בהמשך נלמד, מה התכונות המייחדות נוגדנים המועברים בחיסון סביל זה.
פיתוח תרכיבי חיסון:
החיסון נגד שעלת, הניתן לילדים בישראל במסגרת החיסון המשולש דיפטריה – טטנוס – שעלת, הוא בעל תופעות לוואי קשות. על פי הסטטיסטיקה, אחד ל – 140 אלף ילדים עלול להיפגע בנזק נוירולוגי קבוע בעקבות החיסון.
ש. מדוע, אם כן, צריך לחסן מפני מחלות מדבקות (כמו שעלת)?
פיתוח תרכיב חיסון נגד גורם אלים חייב לענות על הקריטריונים האלה: (1) בטוח- הוא עצמו אינו גורם למחלה ואינו מותיר תופעות-לוואי שליליות. (2) מקנה הגנה לאורך זמן – הוא מפעיל את מנגנון החיסון ומגן מפני חשיפה לגורם האלים במשך מספר שנים; (3) שימושי – מחירו אינו יקר במיוחד, הוא אינו מתפרק עם הזמן והוא קל להזרקה. מבחינה מעשית המטרה העיקרית של המחקר בתורת החיסון הייתה ונשארה פיתוח תרכיבי חיסון נגד מחלות זיהומיות. ההישגים בכיוון זה הם עצומים; מחלות קשות כמו שיתוק ילדים ודיפתריה כמעט חלפו מן העולם. חיסון המוני מצריך מערכת מפותחת של מוסדות רפואיים שיכולים להתגבר על הבעיות הלוגיסטיות הכרוכות בכך. החיסונים הנהוגים כיום בארצות המפותחות, וישראל ביניהן, מסוכמים בטבלה שלפנינו:
| תרכיב חיסון נגד | גורם המחלה | גיל קבלת החיסון (חודשים) | |
|---|---|---|---|
| 1* | דיפתריה (קרמת) | רעלן המופרש על ידי חיידק | 15, 6, 4, 2 |
| טטנוס (צפדת) | רעלן המופרש על ידי חיידק | ||
| שעלת | חיידק | ||
| 2 | שיתוק ילדים | נגיף | 15, 6, 4, 2 |
| 3 | חצבת | נגיף | 12 |
| חזרת | נגיף | ||
| אדמת | נגיף |
תהליך הפיתוח של תרכיבי חיסון קשה וממושך. דוגמאות:
- תהליך הפיתוח של תרכיב חיסון יעיל נגד צהבת מסוג B (hepatitis B) נמשך כ-17שנה, ורק לאחרונה הוא הסתיים בהצלחה.
- תהליכי הפיתוח של תרכיבים יעילים נגד הטפיל הגורם למלריה ונגד נגיף האיידס עדיין נמשכים.
ההבדלים בין המנגנון המולד למנגנון הנרכש מסוכמים בטבלה שלפנינו:
| מנגנון | מולד | נרכש |
|---|---|---|
| הגנה מיידית מפני פולש | כן | לא*[7] |
| מופעל על ידי הפולש | לא | כן |
| תגובתו ספציפית לפולש | לא | כן |
| מותיר זיכרון חיסוני | לא | כן |

[2] אופטימליים- לדוגמה, חשיפת המיקרואורגניזמים לטמפרטורה גבוהה מדי או גידולם במאכסן שונה מהרגיל.
[3] לקריאה נוספת: "ציידי החיידקים" מאת פ' דה קריף.
[4] גחלת – כבר בשנת 1876 זיהה ובודד רוברט קוך את הגורם לגחלת ( Bacillus anthracis ) ואת גורם
לכולרה (Vibrio cholerae ). אולם היה זה פסטר שהצליח לפתח מחיידקים אלה תרכיב חיסון מוצלח.
[5] סרום – כמחצית מנפח הדם מורכב מנוזל שמכונה פלזמה. הפלזמה היא תמיסה מימית של חומרים שונים, כמו חלבונים וגלוקוז. הסרום (serum, או נסיוב) מכיל את כל מרכיבי הפלזמה, למעט חלבונים הקשורים בקרישה.
[6] טבלה 1.3 – קריאה נוספת: (1) תורת החיסון, הוצאת האוניברסיטה הפתוחה 1992 , יחידה 7: חסינות וחיסונים, עמ' -44; (2) עולם החיידקים, הוצאת האוניבריסטה הפתוחה 1991, עמ' 143 – 140.
[7] בתגובה השניונית תיתכן הגנה מיידית מפני הפולש שני מנגנוני ההגנה עובדים יחדיו כדי לסלק פתוגנים מן הגוף.


